Diminutos "corazones" se autoensamblan en platos de laboratorio e incluso laten como los de verdad
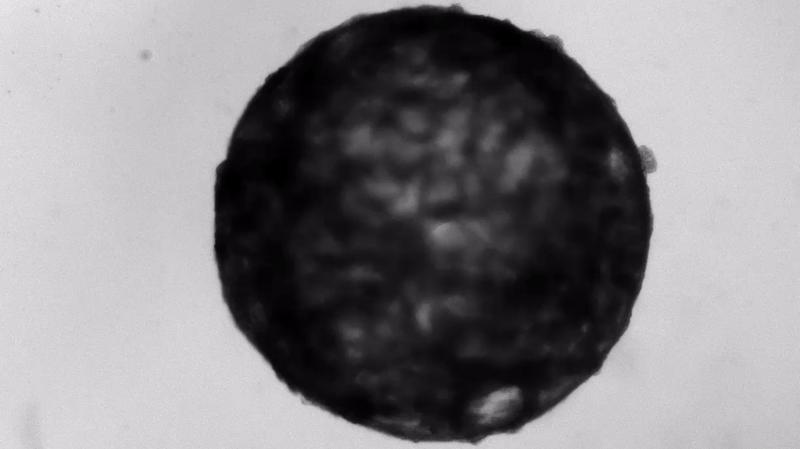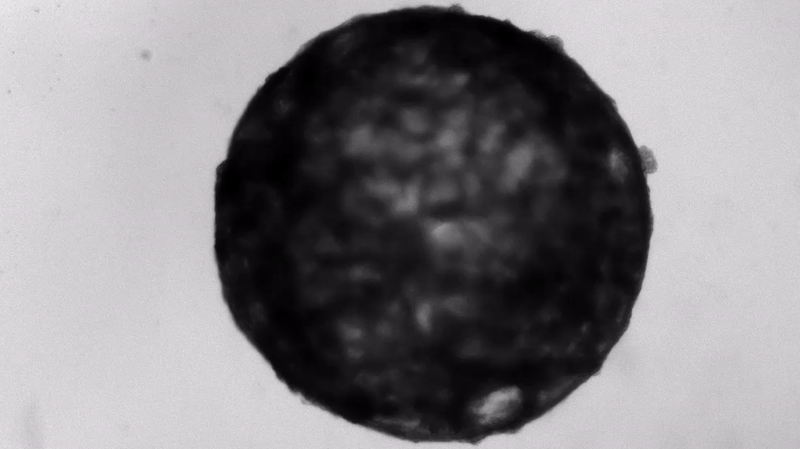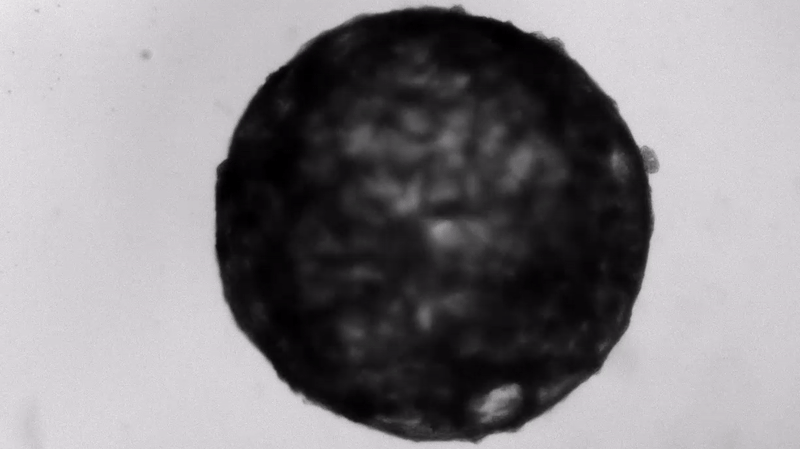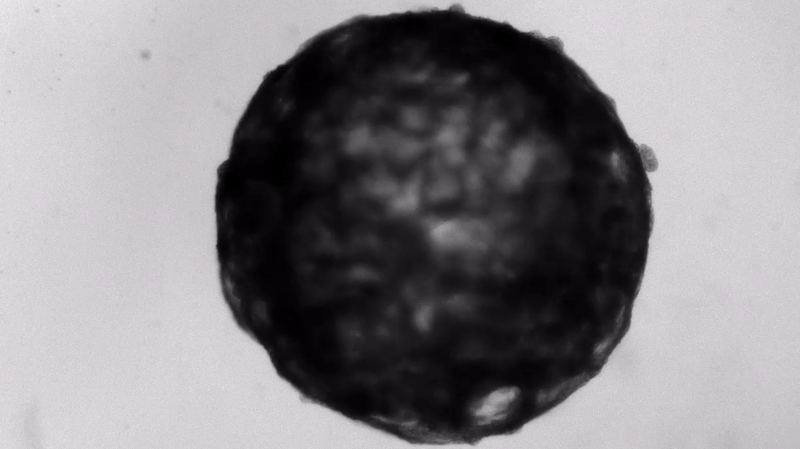
Bajo la atenta mirada de los científicos, las células madre se reunieron en placas de laboratorio para formar pequeños "organoides" de corazón, del tamaño aproximado de una semilla de sésamo, y comenzaron a "latir" como verdaderos corazones en miniatura.
Para guiar a las células madre hacia estas estructuras, el equipo de investigación expuso las células a un conjunto de proteínas y pequeñas moléculas que se sabe que intervienen en el desarrollo temprano del corazón humano en el útero, según un nuevo estudio, publicado el jueves (20 de mayo) en la revista Cell. Estas proteínas y moléculas se acoplaron a los receptores de la superficie celular y desencadenaron una reacción en cadena que hizo que las células madre se diferenciaran en varios tipos de células diferentes que se encuentran en el corazón.
El equipo descubrió que, tras una semana de desarrollo, las células se organizaron en estructuras huecas con forma de cámara, análogas al ventrículo izquierdo del corazón. Además, las paredes de las cámaras empezaron a contraerse rítmicamente, imitando los latidos del corazón humano.
Las vacunas neutralizan la variante del coronavirus de Nueva York en platos de laboratorio
La "hormona del amor", la oxitocina, puede ayudar a reparar corazones rotos (literalmente), según un estudio de laboratorio
11 partes del cuerpo cultivadas en el laboratorio
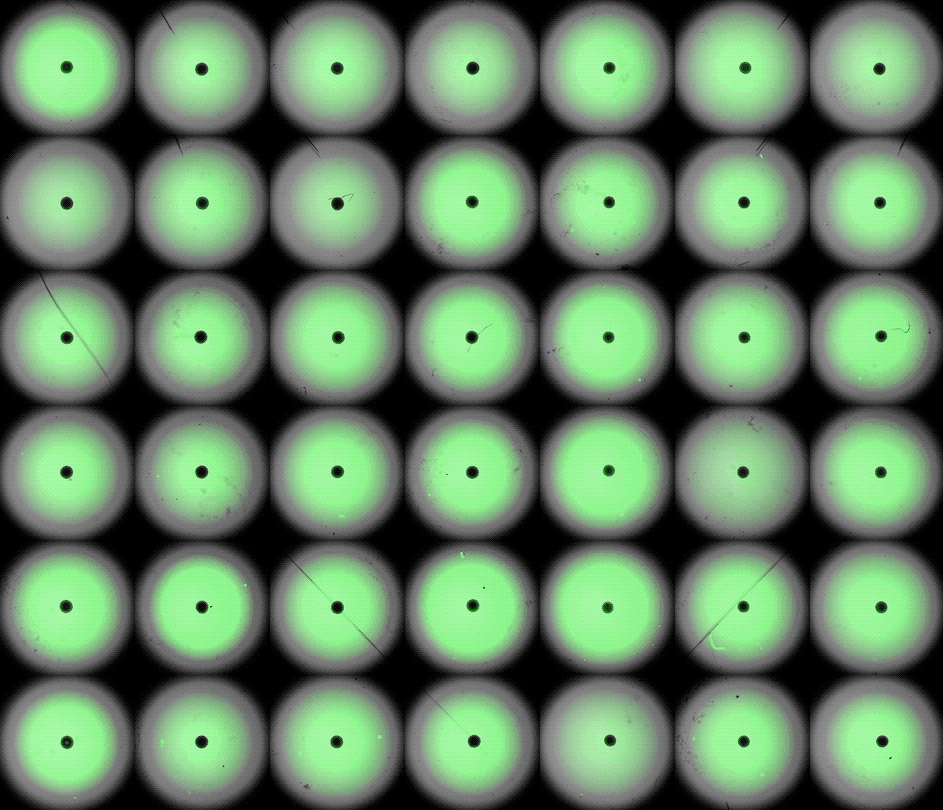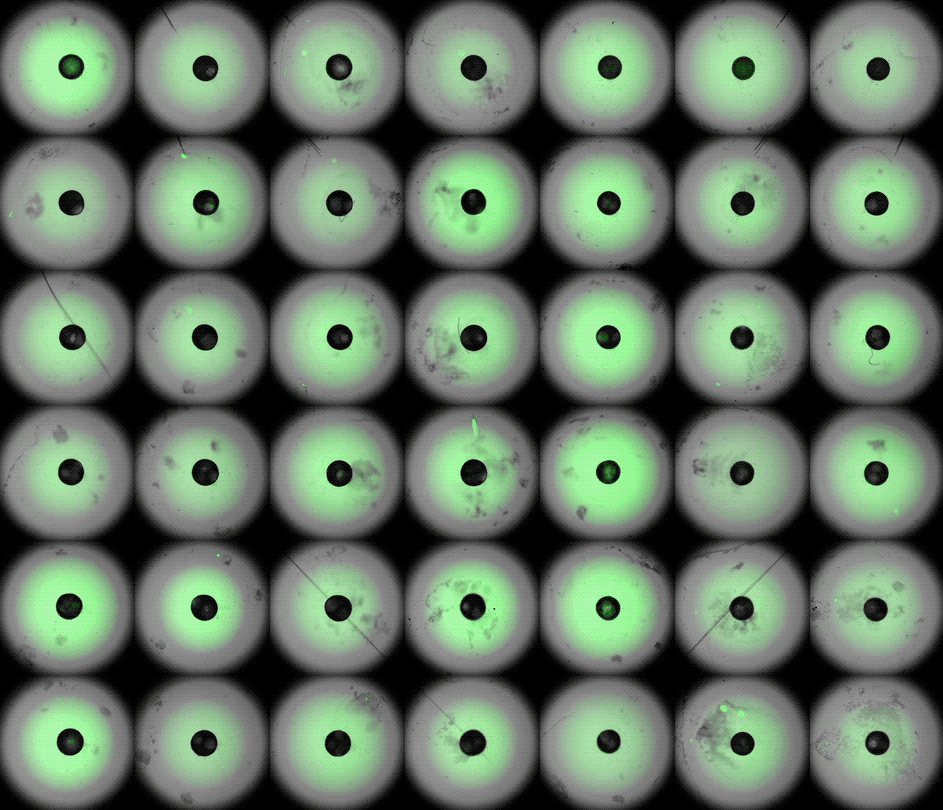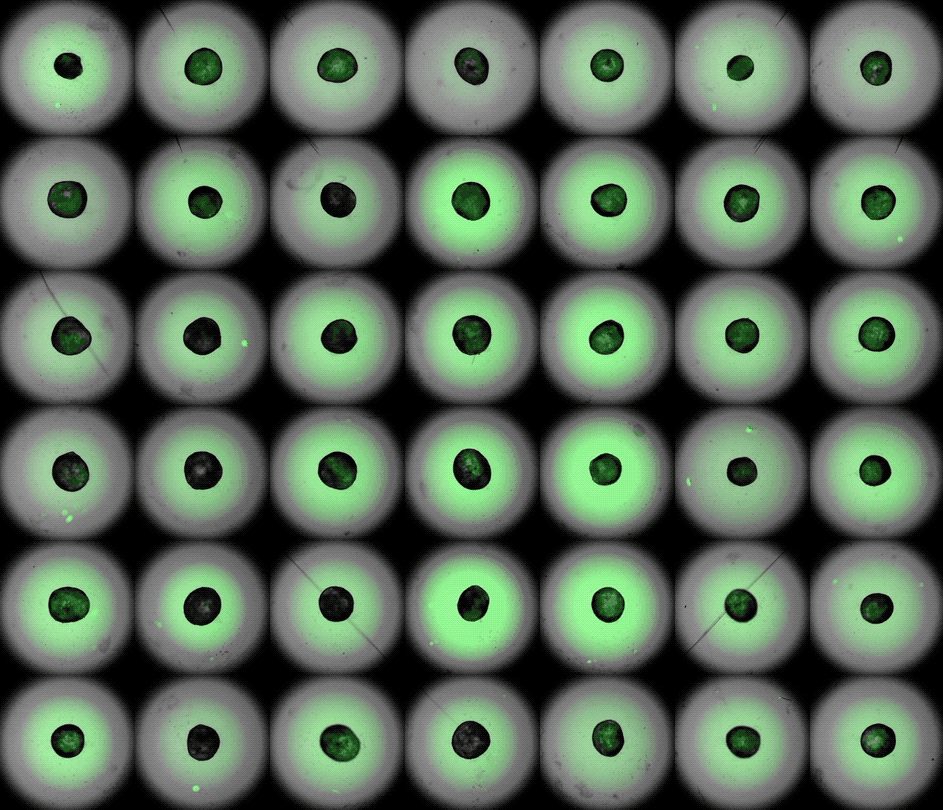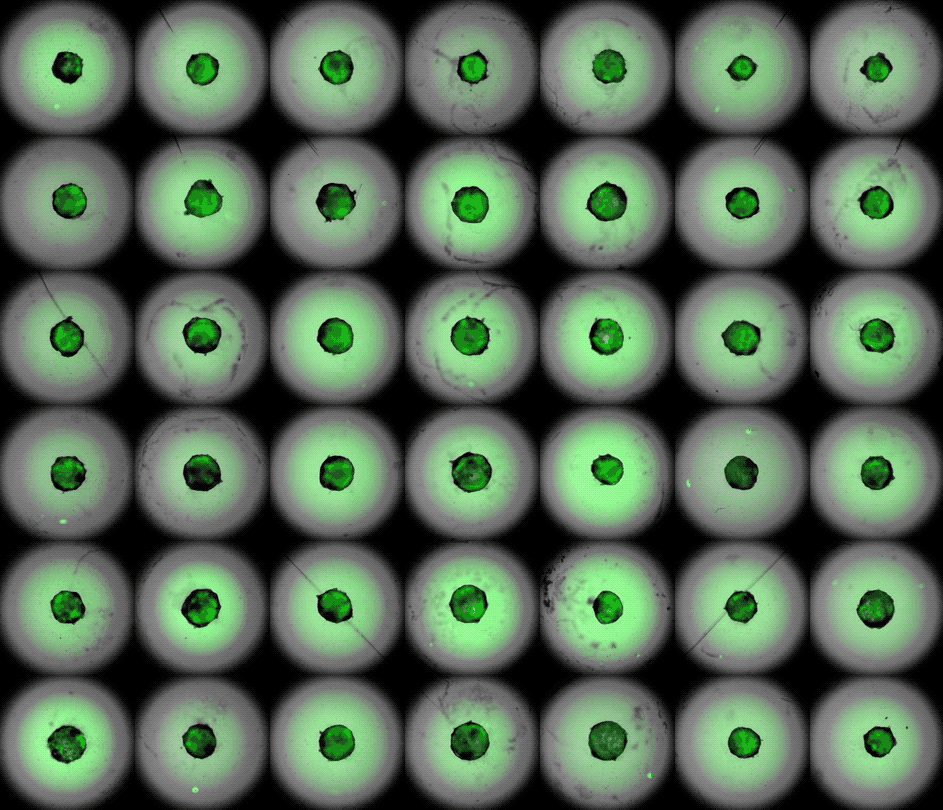
"Lo que nos interesa es básicamente cómo funciona el desarrollo del corazón humano y cómo falla cuando tenemos, por ejemplo, defectos cardíacos congénitos", explica el autor principal, Sasha Mendjan, jefe de grupo del Instituto de Biotecnología Molecular de la Academia Austriaca de Ciencias de Viena. Estos defectos suelen aparecer en una fase bastante temprana del embarazo, pero los científicos no pueden observar directamente los embriones humanos para ver exactamente cómo se producen. "No tenemos acceso a esta ventana: se trata básicamente de una caja negra", explica Mendjan a Live Science.
Ahí es donde entran los diminutos organoides: Pueden proporcionar una visión poco frecuente de estas primeras etapas de desarrollo. El equipo llama a su creación "cardioides", abreviatura de organoides cardíacos. Los cardioides también podrían aportar información sobre algunas afecciones cardíacas del adulto, en las que las células cardíacas lesionadas retroceden a un estado similar al del feto pero no se regeneran como lo harían las células embrionarias, añadió Mendjan.
"Este trabajo es significativo en el sentido de que partieron de cuerpos embrionarios", es decir, grupos de células madre pluripotentes en 3D, un tipo de célula madre que puede dar lugar a muchos tipos de células, dijo Ying Mei, profesor asociado de bioingeniería en la Universidad de Clemson, que no participó en la investigación. En concreto, el equipo consiguió introducir las células en una estructura de cámara hueca, algo que no se había hecho antes con cuerpos embrionarios, dijo Mei.
"Que yo sepa, ésta es la primera".
De grupo de células a cardioide palpitante
En lugar de empezar con una masa de células madre, los científicos también pueden crear organoides utilizando un enfoque llamado ingeniería de tejidos, que implica la construcción de un andamio físico y luego la introducción de células en esa estructura. "Cuando se adopta el enfoque de la ingeniería tisular, se está construyendo algo según un plan, como se sabe que debe ser el órgano final", dijo Mendjan.
"Creo que ambos enfoques tienen sus propias ventajas", señaló Mei. Por ejemplo, Mei y sus colegas crearon un organoide a partir de células cardíacas específicas para simular ataques cardíacos en una placa de laboratorio, según informaron en un informe de 2020 en Nature Biomedical Engineering. Estos organoides construidos como andamios también pueden utilizarse para analizar fármacos, como los diseñados para tratar daños cardíacos, antes de que los medicamentos entren en ensayos con animales o humanos.
Pero, aunque la ingeniería de tejidos puede captar aspectos específicos de una enfermedad, estos organoides no reflejan cómo se desarrollan los órganos reales en el útero, dijo Mei. Los nuevos cardioides desarrollados por el grupo de Mendjan captan mejor este proceso de desarrollo, dijo.
Para transformar sus células madre en blanco en diminutos corazones, Mendjan y su equipo activaron seis vías moleculares en las células; cada vía describe un efecto dominó de actividad dentro de las células que puede ser desencadenado por sustancias químicas específicas. El equipo probó a activar estas seis vías en distintos órdenes y utilizando diferentes cantidades de sustancias químicas activadoras; finalmente, dieron con una combinación que les proporcionó organoides cardíacos diminutos y palpitantes.
"Esencialmente, las células sólo tenían las señales", es decir, las sustancias químicas activadoras, "y a ellas mismas para unirse. Y una vez que se encontraban, sabían lo que tenían que hacer", explicó Mendjan. "Lo que aprendimos de esto es que hay que dejar que las células hagan lo suyo, interferir lo menos posible", proporcionando sólo las señales esenciales y el combustible necesario para que las células sobrevivan en el cultivo.
Los cardioides se asemejan a pequeñas esferas de aproximadamente 1 milímetro de diámetro que se mueven periódicamente, exprimiendo el líquido dentro de sus centros huecos. "Esto sería análogo a una cámara ventricular izquierda humana en el día 28" del embarazo, dijo Mendjan. El ventrículo izquierdo, que posteriormente bombea la sangre oxigenada del corazón al cuerpo, es la primera estructura que se desarrolla adecuadamente en el corazón, dijo.
Tener un bebé: Etapas del embarazo
Con estos diminutos corazones en la mano, el equipo realizó un experimento para modelar las lesiones en los organoides, para ver si imitaban lo que ocurriría en un corazón real. Congelaron partes de los cardioides utilizando una varilla de acero frío, que mataba las células que tocaba; en respuesta, los cardioides enviaron una flota de células llamadas fibroblastos a los lugares lesionados, que luego construyeron un andamio sobre las células muertas para mantener el organoide intacto.
Esta fase inicial del proceso de reparación se ha observado en modelos animales, pero "esta respuesta nunca se había visto in vitro
", es decir, en placas de laboratorio, dijo Mendjan. "Creo que lo vemos por primera vez porque estos cardioides se comportan mucho más como lo haría un órgano real"
-Los 10 datos más sorprendentes sobre tu corazón
-Los 10 mejores miembros inútiles (y otros órganos vestigiales)
Más allá de las verduras y el ejercicio: 5 formas sorprendentes de tener un corazón sano
Dicho esto, el equipo no sabe por qué las cardioides se comportan como lo hacen, añadió. No saben exactamente cómo o por qué las seis vías moleculares atraen a las células madre hacia una estructura similar al corazón. "Hay muchas cosas que aún no entendemos", dijo Mendjan. De cara al futuro, el equipo tiene previsto seguir experimentando con estas vías para determinar qué cambios precisos provocan en las células madre para formar un cardioide.
"Para mí, esa es realmente una pregunta muy interesante: ¿Qué hace que formen la cámara?" dijo Mei, haciéndose eco del sentimiento. Además de desmitificar estas vías moleculares, el equipo está trabajando ahora para obligar a los cardioides a desarrollar múltiples cámaras, como un corazón real de cuatro cámaras.
"No veo grandes obstáculos para que esto se haga realidad", dijo Mendjan. La creación de un cardioide multicámara permitiría al equipo ver el desarrollo de las válvulas cardíacas y el proceso de septación, en el que el corazón divide su cámara única en varias. Muchos defectos cardíacos congénitos surgen en esta fase del desarrollo, por lo que un cardioide de este tipo podría proporcionar una valiosa información sobre estas condiciones, dijo Mendjan.
Por ahora, en el actual modelo cardioide, "están imitando las primeras etapas de la cardiogénesis", señaló Mei. "Muchas enfermedades [congénitas] comienzan en etapas posteriores. Pero hay que empezar por algún sitio".




